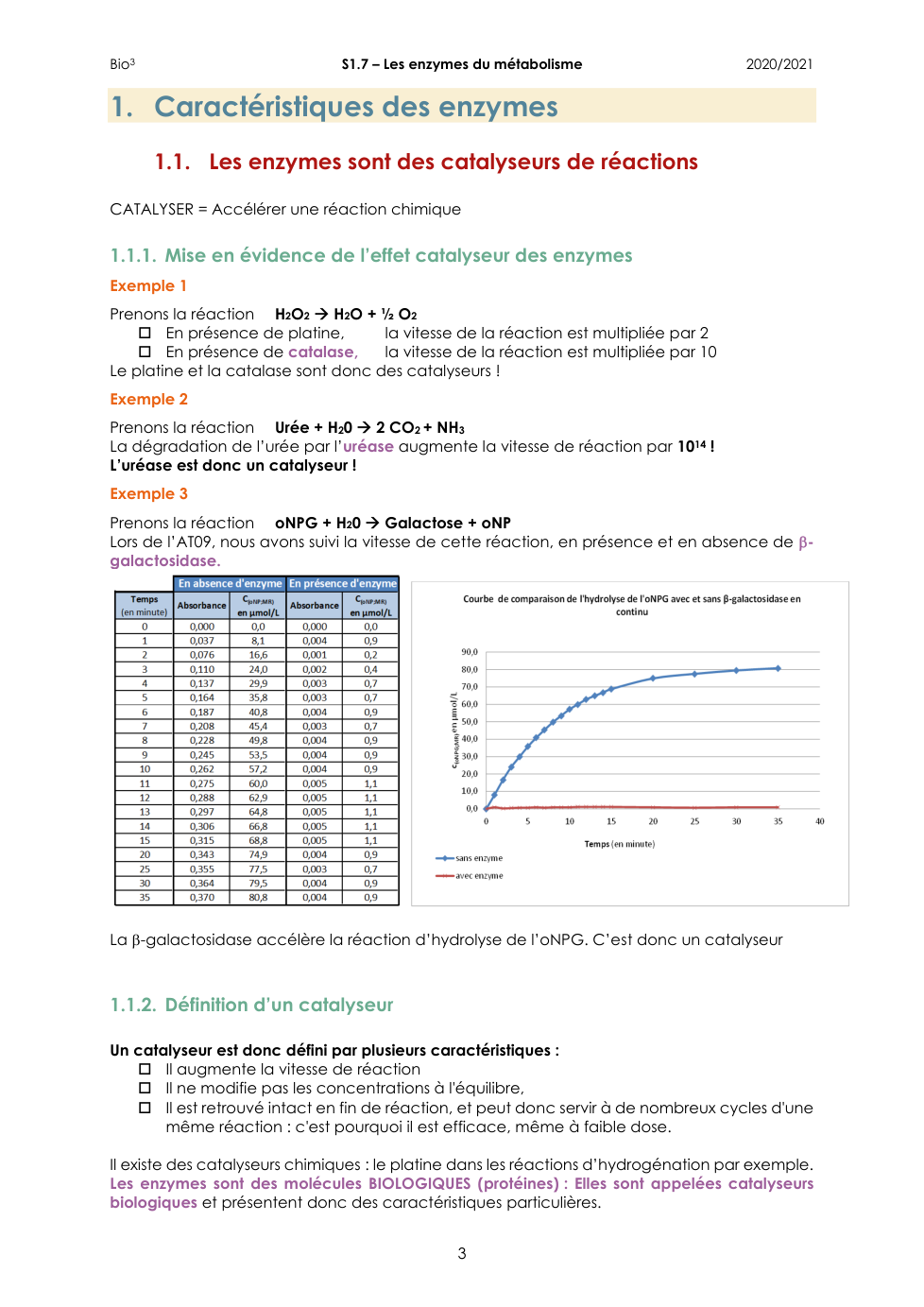
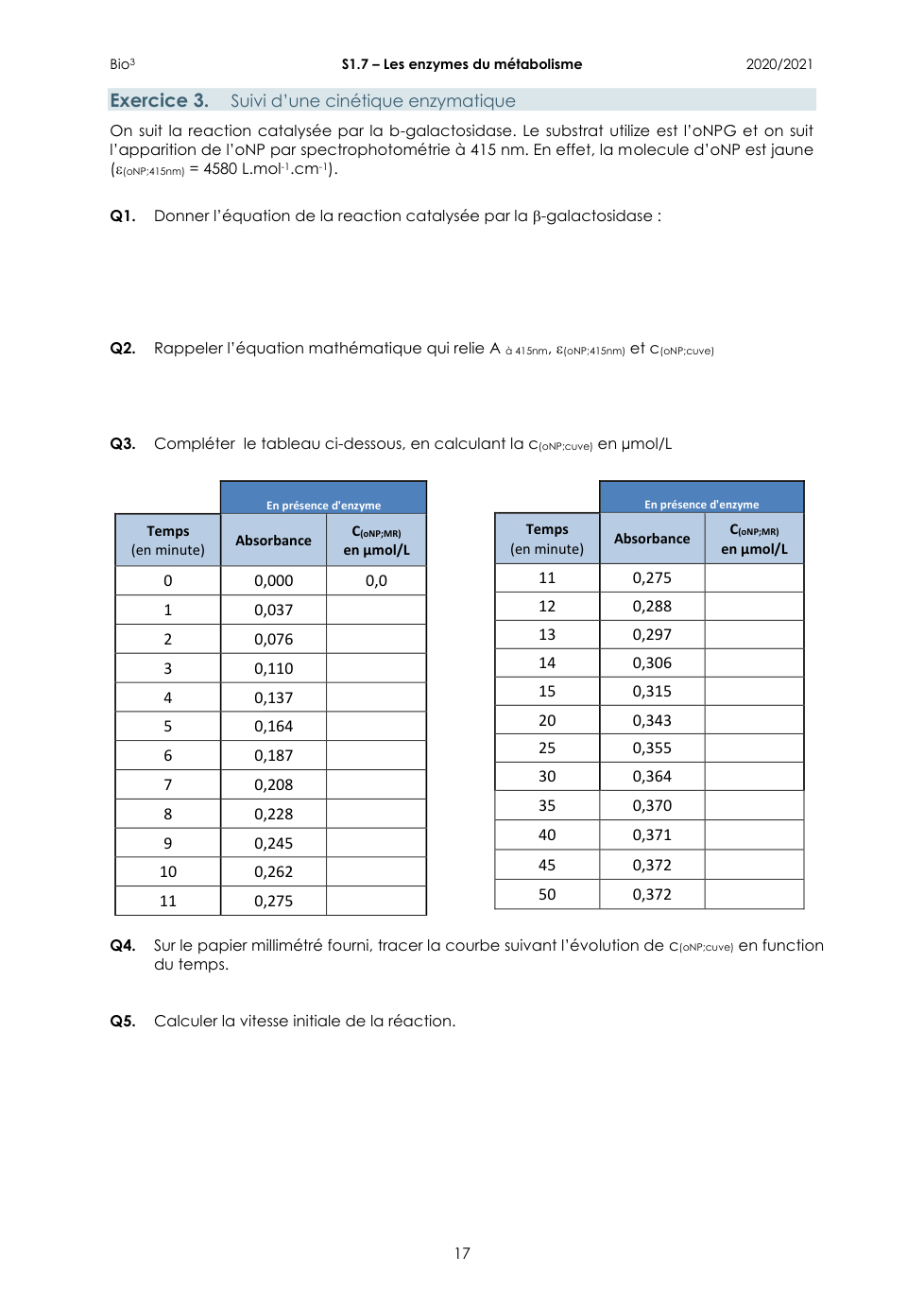
Q3. Compléter le tableau ci-dessous, en calculant la c(oNP;cuve) en μmol/L
En présence d'enzyme
Temps (en minute) Absorbance C(oNP;MR) en μmol/L
0 0,000 0,0
1 0,037
2 0,076
3 0,110
4 0,137
5 0,164
6 0,187
7 0,208
8 0,228
9 0,245
10 0,262
11 0,275
En présence d'enzyme
Temps (en minute) Absorbance C(oNP;MR) en μmol/L
11 0,275
12 0,288
13 0,297
14 0,306
15 0,315
20 0,343
25 0,355
30 0,364
35 0,370
40 0,371
45 0,372
50 0,372